Medicamentos huérfanos: la odisea de tratarse cuando tienes una enfermedad rara
El lugar de residencia, la falta de eficacia o el elevado precio condicionan el acceso a estos fármacos. De los 95 aprobados a nivel europeo, 46 están disponibles en nuestro país.
Cristina (nombre ficticio) vive en una provincia del noroeste de España. Durante siete años, se ha levantado a las 6 de la mañana un lunes sí y un lunes no y ha conducido 400 kilómetros hasta Madrid. Lloviese, nevase o hiciese un sol de justicia. En realidad, Cristina no vive donde está empadronada. Según el padrón municipal, vive en la capital, donde está el hospital que le administra el único medicamento que existe para tratar su enfermedad. Pasa en el Hospital 12 de Octubre cinco horas, cada dos semanas, recibiendo un fármaco que suple en su cuerpo la proteína que su organismo no produce y que causa un debilitamiento progresivo de sus músculos. Después, vuelve a conducir 400 kilómetros hasta su verdadera casa.
Juan e Irene (nombres ficticios) son dos de los hermanos de Cristina. Ambos, al igual que ella, están diagnosticados con la aparición tardía de la enfermedad de Pompe. Juan vive en el norte de la península e Irene en una de las islas. Este simple hecho cambia radicalmente la situación de cada uno de ellos. Myozyme, el medicamento que proporciona esa proteína que les falta, es la razón. Mientras que Irene ha sido tratada en su casa cada quince días desde que fuera diagnosticada en 2006, Juan y Cristina han tenido que falsear su empadronamiento en Madrid durante casi siete años -desde el 2011- para conseguir el tratamiento.
Un mismo medicamento se dispensa en una comunidad autónoma y no en otra. Dentro de una misma provincia, se concede en unos hospitales y no en otros. Esta es la situación en España de los conocidos como medicamentos huérfanos. Huérfanos porque nadie quiere producirlos y, si lo hacen, será por un alto precio. Debido al reducido número de pacientes al que van dirigidos -afectados por enfermedades raras o de baja prevalencia-, estos medicamentos no obtendrán, en teoría, beneficios en el mercado.
Medicamentos Huérfanos
Un medicamento puede clasificarse como huérfano si está indicado para el diagnóstico, prevención o tratamiento de una enfermedad crónica o que amenaza la vida y que afecte a menos de 5 de cada 10.000 personas en la Unión Europea o aquel que sin incentivos es probable que no se venda lo suficiente como para amortizar la inversión.
A diferencia de la mayoría de los medicamentos, las decisiones sobre si un paciente recibe o no un tratamiento con huérfanos las toman las comisiones de farmacia de cada comunidad autónoma o, en su defecto, los comités de farmacia de los propios hospitales. A veces, esta decisión está basada sólo en criterios clínicos. Otras, el elevado precio de los medicamentos huérfanos y su impacto presupuestario condicionan la resolución. En cualquiera de los casos, estos criterios no son homogéneos en toda España: “Con la misma información objetiva se están dando informes de aplicabilidad o de financiación absolutamente dispares en diferentes comunidades autónomas e incluso en la misma comunidad en pacientes con condiciones semejantes”, afirma el doctor Antonio González-Meneses, pediatra responsable de la Unidad de Dismorfología del Hospital Universitario Virgen del Rocío.
Myozyme, una terapia de sustitución enzimática, fue medicamento huérfano hasta 2016. Aunque desde su aprobación en Europa mostraba beneficios considerables en casos de aparición infantil de la enfermedad de Pompe, esto no ocurría con la aparición tardía de la enfermedad, la de Cristina y sus hermanos. Estudios posteriores a la aprobación europea indican que en el inicio tardío de la enfermedad, los beneficios acreditados por el medicamento “se consideran limitados”.
“Asintomática”, dice Cristina. Esta fue la razón que argumentó su hospital de referencia para no someterla a terapia con Myozyme. En 2006, con la entrada de este medicamento huérfano en España, su precio de venta se situó en casi 800 euros por un vial de 50 miligramos. “Dependiendo de la comunidad autónoma donde residas puedes ser muy afortunado o no serlo y tener que buscarte la vida”. Después de un año peleando, Cristina decidió abandonar y optó por probar en Madrid. Allí, la interpretación era distinta: Myozyme estaba indicado para tratarla.
España facilita el acceso a la mitad de los tratamientos aprobados por Europa
Los medicamentos huérfanos son especiales, tanto en precio como en efectividad. La autorización de comercialización está centralizada a través de la Agencia Europea de Medicamentos (EMA, por sus siglas en inglés). Este organismo decide cuáles son los medicamentos para enfermedades raras que se ponen a disposición de los pacientes europeos. No obstante, la negociación del precio de venta la deja en manos de los Estados miembros: cada uno decidirá si entra en el mercado local y a qué precio lo hace.
Fran Garibaldi y Aldurazyme
Aldurazyme es la razón por la que Fran Garibaldi, de 8 años, tiene que pasar en el Hospital Virgen del Rocío de Sevilla cinco horas cada semana. La enfermedad de Fran se llama Síndrome de Hurler y pertenece a un grupo de enfermedades raras conocidas como mucopolisacaridosis de tipo I. Aunque el medicamento no detiene la evolución ni produce mejoras significativas en el desarrollo de la misma, la madre de Fran explica que le funciona bien.
De los 95 medicamentos huérfanos aprobados por la EMA a fecha de abril de 2017, 46 están financiados y comercializados en España, según la información aportada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) a través de una solicitud de acceso a la información pública. En contraste, la Ministra de Sanidad, Servicios Sociales e Igualdad (MSSSI), Dolors Montserrat, declaraba, también en abril, que “son 90 las terapias de medicamentos huérfanos que asume España”. Al intentar corroborar este dato, el Ministerio se ha negado a dar más información alegando que “lo que dice la ministra es el dato oficial”.
“Es cierto que en el último año ha habido un aumento en España de medicamentos huérfanos autorizados, pero hay que distinguir entre la autorización del medicamento y la comercialización del mismo”, señala la eurodiputada socialista y miembro de la Comisión de Medio Ambiente, Salud Pública y Seguridad Alimentaria (ENVI), Soledad Cabezón. La desigualdad con Europa se traslada directamente a los pacientes españoles: aunque un tratamiento esté autorizado, no estará disponible en los hospitales hasta que su comercialización sea efectiva.
El alto precio a pagar
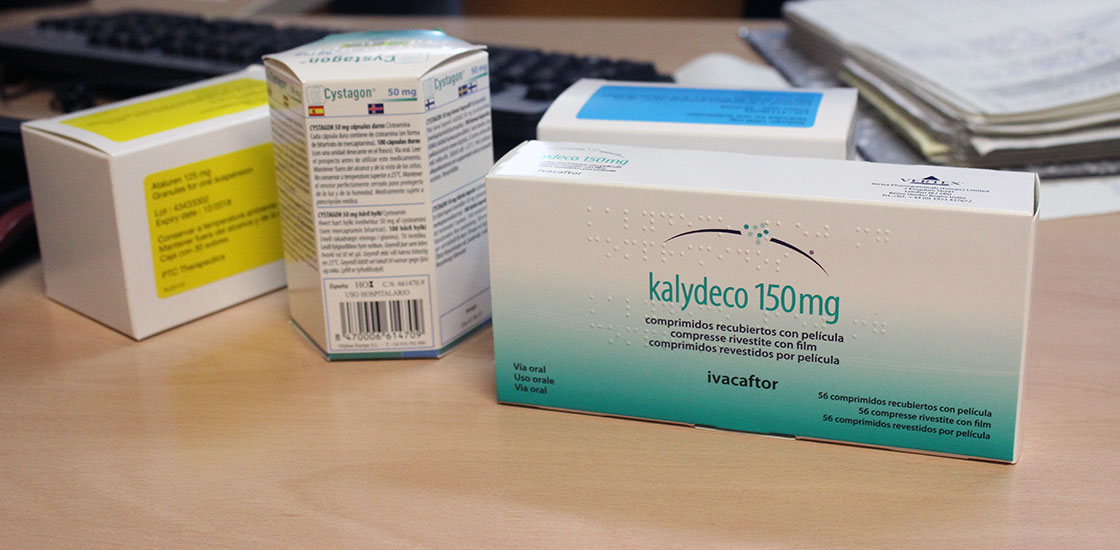
“A mí el Kalydeco me ha cambiado la vida radicalmente”, afirma Gustavo. Este sevillano, de 37 años, tiene un tratamiento de por vida con un medicamento huérfano llamado Kalydeco como consecuencia de la fibrosis quística que sufre. El tratamiento cuesta 225.000 euros al año -más de 18.000 euros la caja de 56 pastillas de 150 miligramos de principio activo- que salen del presupuesto del Hospital Virgen del Rocío de la capital andaluza. Tras conocer los resultados del medicamento en un congreso, la doctora de Gustavo consiguió tramitarlo a través del departamento de farmacia del hospital. “Me permite hacer un deporte moderado, aumentar mi capacidad respiratoria, aguantar el día a día, mi trabajo… Llego a casa y ya no tengo que estar el resto de la tarde en el sofá del cansancio”, cuenta el sevillano.

Gustavo en la entrada del Hospital Virgen del Rocío. | María Álvarez del Vayo
Kalydeco no es el medicamento huérfano más caro en tratamiento por paciente y año, aunque sí es uno de los más caros por envase en la actualidad -el segundo-, según datos aportados por la AEMPS. Lo supera, por ejemplo, Cerdelga, indicado para la enfermedad de Gaucher de tipo I. La caja de 56 cápsulas de 84 miligramos de principio activo tiene un precio de venta de 21.600 euros. El tratamiento de un paciente que necesite dos pastillas al día de Cerdelga costará a un hospital 260.000 euros al año.
Los tratamientos más caros con medicamentos huérfanos
| Medicamento | Enfermedad | Precio estimado del tratamiento anual | Número de veces el gasto farmacéutico hospitalario por persona y año | Precio por caja |
|---|---|---|---|---|
| Cerdelga | Enfermedad de Gaucher de Tipo 1 | 259.183,56€ | 1934x | 21.598,63€ (56 cápsulas de 84 mg) |
| Kalydeco | Fibrosis quística | 225.337,80€ | 1681x | 18.778,15€ (56 comprimidos de 150mg) |
| Vyndaqel | Polineuropatía sintomática en estadio 1 | 139.225,80€ | 1038x | 11.602,15€ (30 cápsulas de 20 mg) |
| Imnovid | Mieloma múltiple | 116.761,80€ | 871x | 9.730,15€ (21 cápsulas de 4 mg) |
| Imbruvica | Linfoma de células del manto (LCM), Leucemia linfocítica crónica (LLC) y Macroglobulinemia de Waldenström (MW) | 110.241,00€ | 822x | 9.186,75€ (120 cápsulas de 140 mg) |
El precio que los laboratorios establecen para los medicamentos huérfanos es uno de los mayores obstáculos para el acceso a este tipo de tratamientos. “La inversión media para desarrollar un medicamento huérfano es de 1.500 millones de euros y se tarda unos 12 años desde la síntesis de un fármaco potencial hasta su comercialización”, asegura la Asociación Española de Laboratorios de Medicamentos Huérfanos y Ultrahuérfanos (AELMHU), cifra que no hemos podido confirmar. No obstante, este tipo de medicamentos cuenta con una serie de incentivos especiales que empujan, desde Europa, su comercialización. Entre ellos, el monopolio de mercado en la indicación a la que va dirigida de 10 años, que en el caso de medicamentos pediátricos llega hasta los 12 años, y que va más allá de la patente: si otro fármaco quiere comercializarse para la misma indicación, tendrá que mostrar beneficios significativos para acabar con ese monopolio.
Eficacia en tela de juicio
El verdadero debate sobre el precio de los medicamentos huérfanos está en los beneficios que demuestran muchos de ellos. “Si un medicamento es totalmente efectivo y está demostrado que es capaz de curar una enfermedad rara, el precio será justificable. Pero si sus resultados están tomados con pinzas, este precio no se va a poder justificar” explica la doctora Marisol Montolio, directora científica de Duchenne Parent Project España y representante europea de pacientes en Eurordis, la organización de pacientes europea de enfermedades raras.
Del total de medicamentos aprobados por la EMA en la actualidad -95 medicamentos en abril de 2017-, 15 tienen una aprobación condicional. Esto significa que se autoriza su comercialización sin tener todos los datos necesarios para una aprobación normal y que, anualmente, el fabricante tendrá que ir entregando a la EMA los datos necesarios para llegar a tener una comercialización “estándar”. Además, otros 13 medicamentos huérfanos tienen el visto bueno de Europa bajo circunstancias excepcionales: el laboratorio no presentó datos completos sobre eficacia y seguridad en el momento de la autorización comercial. Esta se les da de manera excepcional durante 5 años.

Joaquín y Orkambi
“¿Me han oído toser?”, pregunta Joaquín con una sonrisa. “Antes no hubiera podido subir a este piso” afirma. Joaquín toma Orkambi desde el 2016 para tratar la fibrosis quística que sufre. Es una enfermedad rara, hereditaria y potencialmente mortal que provoca la acumulación de moco espeso y pegajoso en los pulmones, el tubo digestivo y otras áreas del cuerpo. Aunque está autorizado por la Agencia Europea de Medicamentos no está aún comercializado en España. Joaquín lo toma por la vía especial de acceso a medicamentos conocida como uso compasivo.
Los estándares de aprobación de la EMA para los medicamentos huérfanos han sido criticados en varias ocasiones. Una investigación científica del año 2014 publicada en el British Medical Journal, concluye, tras analizar 74 medicamentos huérfanos, que “mientras unos medicamentos han demostrado evidencia de beneficios significantes, otros carecen de evidencia en efectividad e, incluso, algunos están asociados con efectos secundarios severos”. Otro estudio ya había llegado en 2013 a conclusiones similares tras evaluar 64 medicamentos.
“La labor de la EMA no es medir el impacto socio-económico del medicamento, su labor es exclusivamente científica” defiende el director de la Federación europea del síndrome de Dravet y observador en el Comité de Medicamentos Huérfanos (COMP, por sus siglas en inglés), Julián Isla. Y añade: “La EMA es el policía que está en la frontera y decide quién pasa, pero no tiene que estar pensando: ‘este entra y después va a ser un delincuente’. De eso se encarga la policía que esté dentro, porque entonces no entraría nadie”. Isla defiende que “la discusión no es EMA sí o EMA no, la discusión es cómo abaratar los costes del desarrollo de estos fármacos.”
En España, existen visiones que defienden que el debate sobre financiación o no de un medicamento huérfano debería tener en cuenta criterios especiales: “Debe plantearse qué otros criterios considerar para conciliar la sostenibilidad del sistema sanitario con las preferencias de la sociedad”, concluía una investigación realizada por la Agencia de Evaluación de Tecnologías Sanitarias (AETS) del Instituto de Salud Carlos III en 2016.
El “gran agujero” del presupuesto hospitalario
Cristina y su hermano Juan han estado recibiendo tratamiento con Myozyme en la Comunidad de Madrid desde 2011. En esta comunidad, el gasto en medicamentos huérfanos llegó a 88 millones de euros en 2016 -la mayor suma desde 2012. En total, supone un 9% del presupuesto para adquisición de productos farmacéuticos del Servicio Madrileño de Salud para ese mismo año. Este coste compite directamente con el techo de gasto para los medicamentos no huérfanos de las comunidades autónomas y los hospitales. En estos últimos, “generalmente producen un gran agujero en los presupuestos”, explica el director de la Fundación Mehuer, Manuel Pérez.
“Ante esta situación compleja de impacto económico y presupuesto cerrado se debe garantizar el acceso y la equidad de los tratamientos a toda la población, pero siempre teniendo presente las limitaciones en el gasto público y fomentando la sostenibilidad del sistema” explicaba la jefa de Servicio de Farmacia del Hospital Universitario La Paz de Madrid, Alicia Herrero, en su ponencia en las I Jornadas de Enfermedades Raras y Medicamentos Huérfanos.

David y Kuvan
David es un niño de 9 años que desde los 9 meses tiene un tratamiento con medicamento huérfano por la enfermedad rara hereditaria conocida como fenilcetonuria o PKU. Su padre, Manuel (en la foto), tiene que ir a recoger sus medicinas cada cinco días. Los afectados como David tienen problemas con el procesamiento en una fracción de las proteínas, la fenilalanina, presente en muchos de los alimentos de origen animal. Al no poder procesarse correctamente, la fenilalanina se acumula en la sangre causando un daño progresivo en el sistema nervioso. Para combatirlo, David toma Kuvan, el medicamento huérfano que contribuye a reducir la concentración de fenilalanina en la sangre. El fármaco está financiado en España desde 2009, con precio de venta al público (PVP) de 2.741€ -la caja de 120 comprimidos de 100 mg.
Para conseguir ese acceso igualitario y justo, el Grupo Parlamentario Ciudadanos presentó una Proposición no de Ley en el 2016 que garantizaría, según ellos, la equidad sanitaria de personas con enfermedades raras en todo el territorio nacional. El técnico de sanidad de este Grupo Parlamentario, Ricardo Pérez, declara que el problema es “la falta de atención de las autonomías a este problema”. Además, señala: “Como son tan pocas personas, no es un reto electoral. Es decir, si tienes que invertir 200.000 euros en un fármaco que van a utilizar cuatro personas o en uno que van a utilizar 1.500 personas, ¿cuál es el que te da más votos?”. Esta proposición ha llegado a acuerdo en la Comisión de Sanidad del Congreso de los Diputados.
Junto a estas proposiciones políticas, son varias las posibles soluciones que se presentan: partidas autonómicas –como propone AELMHU- o cambiar la dispensación hospitalaria de algunos tratamientos por la dispensación en farmacia comunitaria –como propone Santiago Cuéllar del Consejo General de los Colegios de Farmacia. “Lo que hay que tener claro es que si se considera que hay que autorizar este tipo de medicamentos, una vez que se autoriza su comercialización habrá que establecer mecanismos correctos para que lleguen a todos los pacientes en igualdad de condiciones”, sentencia el doctor Meneses-González.
“Lo que me ha hecho tanto daño es el abandono”, cuenta Cristina. El primero de mayo ha comenzado a recibir su tratamiento con Myozyme en su localidad. Después de siete años, Cristina se trata donde está su familia, su trabajo y sus amigos.
Metodología
Los datos aportados por la Agencia Europea del Medicamento en su página web nos sirvieron para agrupar todos los documentos publicados de cada uno de los medicamentos huérfanos aprobados a nivel central. Se obtuvieron, también, datos relativos a las reuniones del Committee of Orphan Medicine Products (COMP) donde se señalan el número de designaciones. A nivel español, se extrajeron los datos relativos a los medicamentos huérfanos publicados en la página web CIMA de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS).
No obstante, para conocer la complejidad del sistema a nivel español, necesitábamos más datos no publicados. Por esta razón se realizaron peticiones de información a nivel estatal, todas al Ministerio de Sanidad, Servicios Sociales e Igualdad (MSSSI). Con estas peticiones se consiguió el número de medicamentos huérfanos comercializados y financiados a fecha de abril de 2017. El número, sin embargo, no correspondía con el extraído de la página web de CIMA. El Ministerio se negó a resolver la disparidad de números en sus propios datos, por lo que el número final de medicamentos huérfanos que se trata en esta investigación es en referencia a lo facilitado en la solicitud de información.
Para calcular la estimación de precio por tratamiento/año se utilizó la posología indicada en la ficha técnica europea de cada medicamento.
Para calcular el gasto en farmacias hospitalarias por persona y año se ha dividido el gasto total de 2016 que publica el Ministerio de Hacienda y Función Pública entre el número de habitantes de España a fecha de 01/01/2017 indicado en el Instituto Nacional de Estadística (INE).
Nota
Este trabajo es fruto de la investigación desarrollada durante el Máster de Periodismo de Investigación, Datos y Visualización de la Universidad Rey Juan Carlos y Unidad Editorial. La investigación ha tenido el apoyo de Caixabank y el asesoramiento de la Comisión Europea en España. La edición corrió a cargo de Marta Ley, profesora en el Máster y periodista de datos en El Mundo Data.
Déjanos decirte algo…
En esta información, y en todo lo que puedes leer en Civio.es, ponemos todo el conocimiento acumulado de años investigando lo público, lo que nos afecta a todos y todas. Desde la sociedad civil, 100% independientes y sin ánimo de lucro. Sin escatimar en tiempo ni esfuerzo. Solo porque alguien tiene que hacerlo.
Si podemos informar así, y que cualquiera pueda acceder sin coste, sin barreras y sin anunciantes es porque detrás de Civio hay personas comprometidas con el periodismo útil, vigilante y al servicio de la sociedad en que creemos, y que nos gustaría seguir haciendo. Pero, para eso, necesitamos más personas comprometidas que nos lean. Necesitamos socios y socias. Únete hoy a un proyecto del que sentir orgullo.
Podrás deducirte hasta un 80% de tu aportación y cancelar cuando quieras.
¿Aún no es el momento? Apúntate a nuestro boletín gratuito.